Olá, pessoal!
Sabemos que a Química é a ciência que estuda a matéria. Você também já deve ter ouvido que a matéria é formada por átomos. Na aula de hoje, tentaremos entender o que vem a ser um átomo. De que um átomo é formado? Será que um átomo pode ser dividido? É isso que estudaremos a partir de agora.
Vamos nessa!

Para ter uma noção do que vem a ser um átomo, analisaremos algumas ideias de quatro importantes personagens no estudo da constituição da matéria: Dalton, Thomson, Rutherford e Bohr.
Obs.: Em seu livro didático, as ideias desses personagens são analisadas nas seguintes páginas:
76 a 83 88 a 90
O vídeo disponibilizado no link abaixo ajudará você a entender melhor o que esses personagens pensavam acerca do átomo. Na sequência, apresenta-se um resumo dos modelos atômicos estudados na aula de hoje.
https://www.youtube.com/watch?v=kgg9sdpoKkQ
• Modelo atômico de Dalton
De acordo com esse modelo, a matéria é constituída de pequenas partículas esféricas, maciças e indivisíveis denominadas átomos.

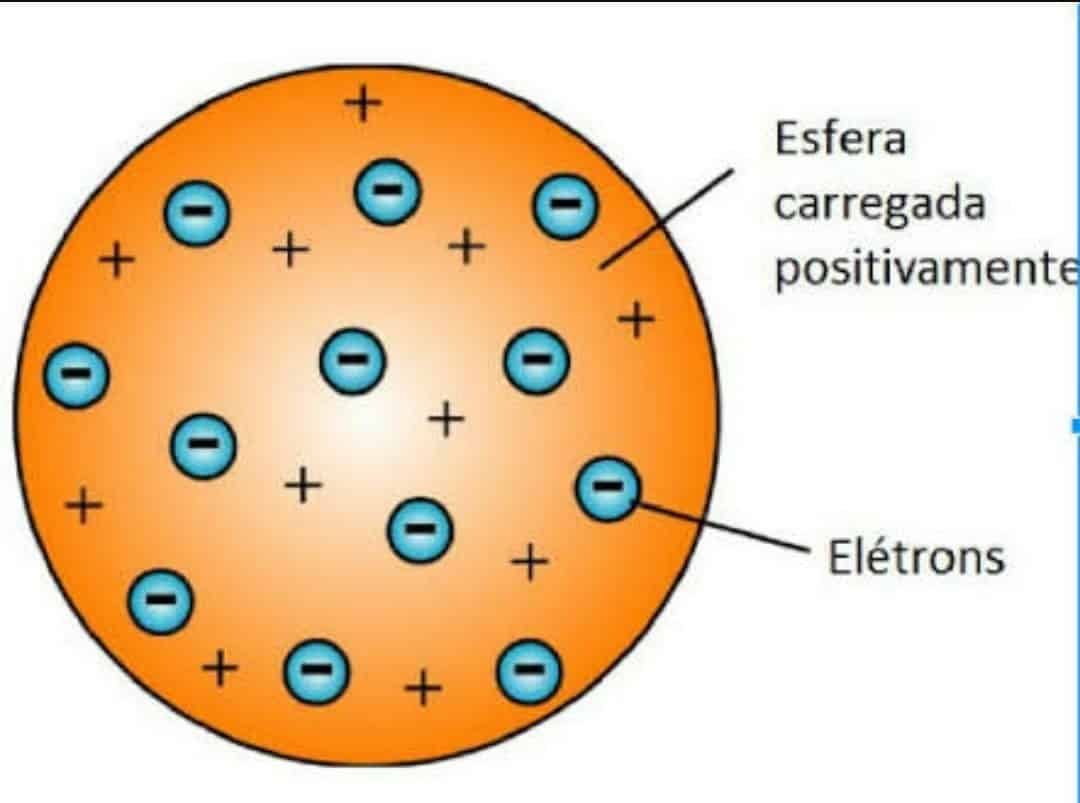
• Modelo atômico de Thomson
Segundo as ideias apresentadas por Thomson, o átomo é maciço, esférico e formado por um fluido com carga positiva, no qual estavam dispersos os elétrons.
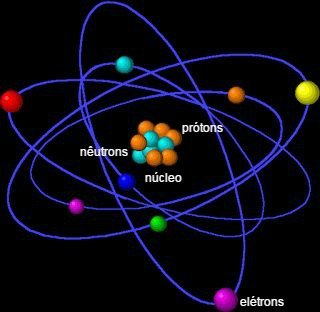
• Modelo atômico de Rutherford
O átomo deve ser constituído de duas regiões distintas:
a) Uma região central, que contém praticamente toda a massa do átomo e apresenta carga positiva, denominada núcleo.
b) Uma região praticamente sem massa envolvendo o núcleo, que apresenta carga negativa, denominada eletrosfera.
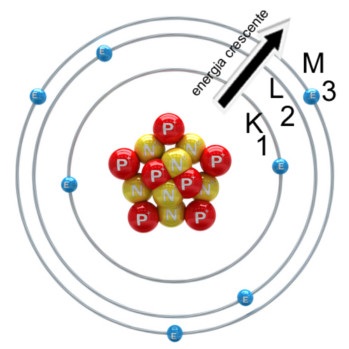
• Modelo atômico de Rutherford-Bohr
Os elétrons descrevem órbitas circulares ao redor do núcleo.
Cada uma dessas órbitas tem energia constante. Os elétrons que estão situados em órbitas mais afastadas do núcleo apresentam maior quantidade de energia.
Quando um elétron absorve certa quantidade de energia, salta para uma órbita mais energética. Quando ele retorna à sua órbita original, libera a mesma quantidade de energia na forma de onda eletromagnética.
ATIVIDADE DE AVERIGUAÇÃO DE APRENDIZAGEM
Obs.: O aluno deve responder às questões a seguir em seu caderno, utilizando caneta, e enviar foto das respostas para o professor, até o dia 04/08/2020. As respostas devem ser justificadas.
1) O átomo de Rutherford (1911) foi comparado ao sistema planetário: núcleo – sol; eletrosfera – planetas.
Eletrosfera é a região do átomo que:
a) contém as partículas de carga elétrica negativa.
b) contém as partículas de carga elétrica positiva.
c) contém nêutrons.
d) concentra praticamente toda a massa do átomo.
e) contém prótons e nêutrons.
2) Considere as afirmativas:
I. O átomo é maciço e indivisível.
II. O átomo é um grande vazio com um núcleo muito pequeno, denso e positivo no centro.
I e II pertencem aos modelos atômicos propostos, respectivamente, por:
a) Dalton e Thomson.
b) Rutherford e Bohr.
c) Bohr e Thomson.
d) Thomson e Rutherford.
e) Dalton e Rutherford.
3) (UCS-RS) Uma semelhança entre os modelos atômicos de Dalton e de Thomson está no fato de ambos considerarem que o átomo:
a) é constituído por prótons, nêutrons e elétrons.
b) é maciço.
c) apresenta elétrons em camadas.
d) é semelhante ao sistema solar.
e) possui núcleo e eletrosfera.
4)Thomson determinou, pela primeira vez, a relação entre a massa e a carga do elétron, o que pode ser considerado como a descoberta do elétron. É reconhecida como uma contribuição de Thomson ao modelo atômico:
a) o átomo ser indivisível.
b) a existência de partículas subatômicas.
c) os elétrons ocuparem níveis discretos de energia.
d) os elétrons girarem em órbitas circulares ao redor do núcleo.
e) o átomo possuir um núcleo com carga positiva e uma eletrosfera.
5) O átomo é a menor partícula que identifica um elemento químico. Ele possui duas partes, a saber: uma delas é o núcleo, constituído por prótons e nêutrons, e a outra é uma região externa – a eletrosfera –, por onde circulam os elétrons. Alguns experimentos permitiram a descoberta das partículas constituintes do átomo. Em relação a essas características, indique a alternativa correta.
a) Prótons e elétrons possuem massas iguais e cargas elétricas de sinais opostos.
b) Entre as partículas atômicas, os elétrons têm maior massa e ocupam maior volume no átomo.
c) Entre as partículas atômicas, os prótons e os nêutrons têm maior massa e ocupam maior volume no átomo.
d) Entre as partículas atômicas, os prótons e os nêutrons têm mais massa, mas ocupam um volume muito pequeno em relação ao volume total do átomo.
e) Entre as partículas atômicas, os elétrons são as de maiores massas.
